-
光学相干断层成像(OCT)是一种生物医学光子成像技术,最早于1991年由David Huang等人提出,其具有无创、非侵入性、实时活体检查等优点,可达微米级超高分辨力[1]。由于人眼组织具有较好的透光性,故OCT技术在眼科光学领域取得了巨大的发展并成功的应用于眼科疾病的诊断[2-5]。但是,眼科OCT设备的评价手段及标准化评定工作进展相对滞后,国际上,美国标准与技术研究院(NIST)、英国国家物理实验室(NPL)与美国食品药品监督管理局(FDA)最早于2009年开始开展OCT设备计量的相关工作,韩国标准研究院(KRISS)和新加坡国家计量中心(NMC)近几年才开始关注该研究领域。2009年,NPL生物光子学研究组研制出用于评价OCT成像分辨率的点扩散函数模体,并系统地分析了其评价效果[6]。2010年,FDA的Agrawal等将纳米粒子嵌入透明的硅树脂基质中,通过分析OCT三维图像,实现了亚微米尺度的轴向和横向分辨率评价[7]。2013年,Pfefer等人测试了三种点扩散函数模体的掺杂颗粒,对比了其在OCT系统的分辨率和信号强度评价方面的性能差异[8]。2014年以来,中国计量科学研究院(NIM)紧跟国际步伐,开展OCT设备的计量研究工作,先后研制了三维分辨率测试模拟眼[9]、层状结构模拟眼[10]、点扩散函数模体[11]和眼后节一体化多参数校准模拟眼[12]等OCT设备计量校准装置。同时,参与制定了第一个OCT国际标准ISO 16971《眼科仪器 眼科光学相干断层扫描仪》[13],并于2015年发布实施。近年来,3D打印技术作为一种快速发展的柔性制造技术已达到亚微米级精度,在眼科模体制造上被广泛使用。2018年,Kedia等人使用双光子聚合方法制作微米级尺寸的仿视锥细胞模体,实现自适应光学OCT系统的横向分辨率计量[14]。2020年,Lamont等利用双光子直接激光写入法,在掺杂二氧化钛粒子的模体中实现了不同视场角小于4 μm的光学分辨率验证[15]。2021年,Horng等人利用相同的技术制作了包含10 µm直径微流体通道的视网膜模体,用于OCT血管造影技术的测试[16]。
现行国际标准ISO 16971提出了对分辨率、视场角、信噪比等一些OCT设备关键参数的测试要求及方法,但随着新兴OCT技术与设备的不断发展,国际标准也面临计量参数和方法在准确性、适用性和便捷性等方面的改进。同时,国内行业标准尚未制定,测试方法的缺失对OCT设备厂家、第三方检测机构和相关计量部门的质检工作带来巨大挑战,故OCT设备的计量标准化问题亟需解决。
文中旨在结合相关国际标准推荐的检验方法,基于3D打印技术设计并制作一种模拟真实人眼结构的模拟眼,旨在对眼科OCT设备进行性能评估。该模型基于Gullstrand I号模型眼简化形成,包括角膜、前房、晶状体、玻璃体和视网膜五个部分,可对横向和轴向分辨率、视场角、图像匹配度、深度测量准确性等关键参数进行计量校准。同时,在设计时充分考虑模拟眼关键设计参数的量值溯源方法,确保其量值可溯源。
-
分辨率是眼科OCT设备的一项关键参数,决定设备对被测样品细节的分辨能力,对微观结构的成像质量起决定性作用。由OCT技术原理可知,其横向分辨率与轴向分辨率相互独立:横向分辨率δxy受限于衍射极限,主要取决于光源中心波长和物镜数值孔径(NA),其表达式详见公式(1);轴向分辨率δz取决于光源中心波长和其相干长度,其表达式详见公式(2):
$$ {\delta _{xy}} = \frac{{\sqrt {2\ln 2} }}{\pi } \cdot \frac{{{\lambda _0}}}{{NA}} $$ (1) $$ {\delta _z} = \frac{{2\ln 2}}{\pi } \cdot \frac{{\lambda _0^2}}{{\Delta \lambda }} $$ (2) 式中:λ0为光源中心波长;Δλ为光源带宽[17]。
-
视场角是眼科OCT设备视野范围的技术指标,定义为被测物体成像过程中可通过光学仪器镜头的最大边缘与镜头中心连线形成的夹角[13]。在眼科OCT扫描模式下记录视场宽度y,则扫描视场角(FOV)可表达为:
$$ {{FOV}} = 2{\text{arctan }}\left(\frac{y}{{2f}}\right) $$ (3) 式中:f为扫描物镜的焦距。
-
眼科OCT能提供眼球剖面结构及其尺寸信息,轴向所测尺寸的准确性是一项关键计量指标。深度测量准确性参数用来评价眼科OCT设备在测量眼球结构尺寸的绝对量值准确性,对医学中判断病变尺寸至关重要。
-
眼科OCT设备一般都可提供眼底图像预览。眼底预览图像成像一般是基于可见光的CCD成像,而光学断层扫描成像是基于近红外光的相干成像,眼科医生会通过直观的眼底图像去定位需要OCT扫描的区域,最后通过OCT图像分析病情。因此,OCT扫描图像与眼底预览图像的匹配程度将直接影响临床上医生对病灶位置的准确判断。
-
设计模拟眼的屈光特性模拟真实人眼屈光组织,设有角膜、前房、晶状体、玻璃体腔和视网膜结构。基于人眼眼球参数,具体光学技术参数如下:(1) 角膜前表面曲率7.60 mm、后表面曲率4.9 mm、厚度0.50 mm;(2) 前房厚度2.41 mm;(3) 晶状体前表面曲率10.46 mm、后表面曲率−12.73 mm、厚度4.50 mm;(4) 玻璃体厚度17.63 mm;(5) 视网膜曲率半径−12.50 mm;(6) 眼轴长设计值25 mm。屈光特性模拟实际人眼屈光组织,等效空气焦距17 mm,眼模型主要参数详见表1。
表 1 所设计的眼模型主要参数
Table 1. Main parameters of designed eye model
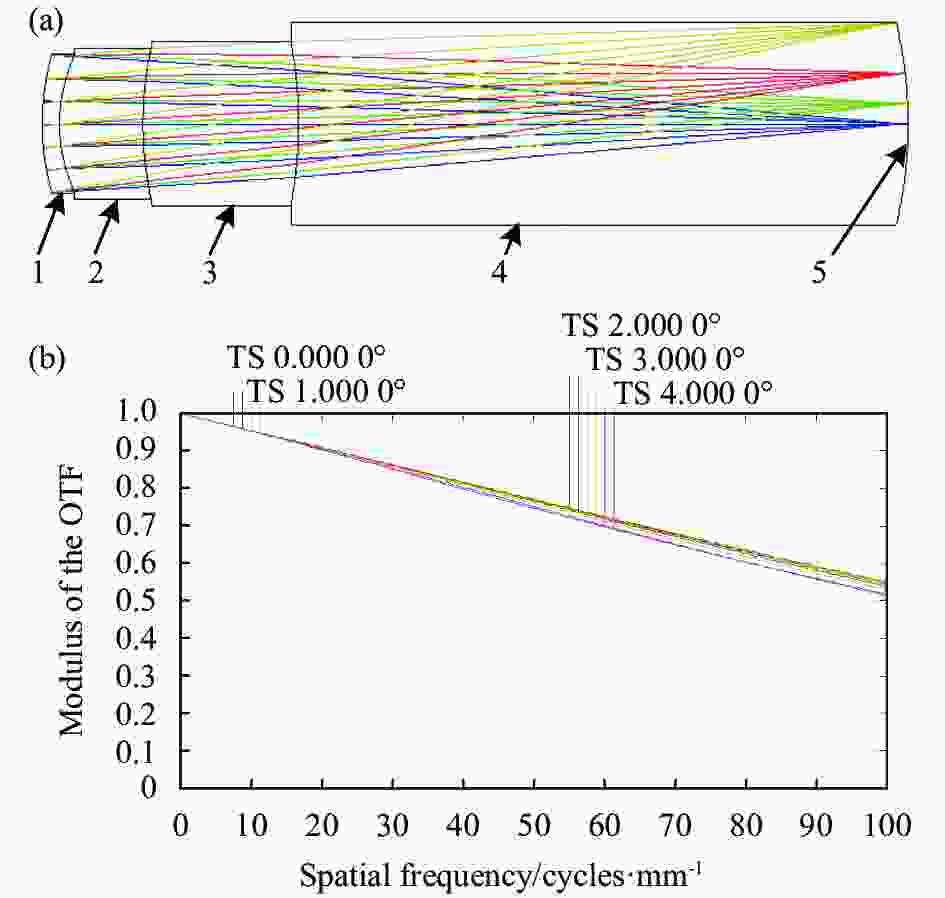
Eyeball tissue Parameters Radius of curvature Thickness Refractive index Anterior surface of cornea 7.60 0.50 1.526 Posterior surface of cornea 4.90 Anterior chamber - 2.41 1.333 Anterior surface of lens 10.46 4.50 1.526 Posterior surface of lens −12.73 Vitreous - 17.63 1.333 Retina −12.50 - - 基于上述条件采用ZEMAX软件进行光学设计,预设参数Gen (孔径)参考人眼清晰视物时瞳孔直径2~5 mm,设计入瞳直径4 mm;预设参数Fie (视场)参考实际人眼清晰感光区域5°~8°,设计最大视场2ω=20°;预设参数Wav (波长)参考医用眼科设备常用近红外波长830 nm。设计的眼模型光路图如图1所示,1-角膜和3-晶状体,采用H-K9玻璃材料,使用光学加工工艺制作;2-前房和4-玻璃体腔,填充介质为水;5-视网膜,使用精密机加工制作。优化后眼模型光学系统评价函数0.20、对应人眼清晰视场的0°~8°的MTF曲线在100 lp/mm处的值均大于0.5 (如图1(b)所示,半视场0°~4°)、焦距16.99 mm、轴长25.03 mm,各项指标满足设计要求,具有良好的光学特性。
-
设计并加工了一种能够为眼科OCT设备提供分辨率参数检测的三维分辨率板,测试图案基于USAF1951靶板、经微纳3D打印技术制作。不同于传统USAF1951靶板的二维平面图案,它不仅能够检测横向分辨率,还可用于轴向分辨率的检测。
三维分辨率板使用深圳摩方材料科技有限公司Nano Arch S130系统,选用浅黄色高精度硬性树脂GR材料进行微纳3D打印,平面设计图如图2 (a)所示。基于1951 USAF设计横向分辨率靶板:共设计六组测标,每组测标由三对横向与纵向垂直排列的长条图案组成,各组测标线宽设计值100、50、25、20、12.5、10 μm,长宽比5∶1;同时设计五组线宽100 μm、长宽比5∶1、高度递减的凸台用于轴向分辨率测试,高度依次为50、30、20、10、5 μm,设计三维图如图2 (b)所示。加工完成的三维分辨率板通过商用眼科OCT设备成像,结果如图2 (c)所示。
-
眼模型的机械设计应满足上述光学设计且可安装3D打印分辨率板,同时具有操作简单、稳定性强等特点。模拟眼机械设计剖视图和实物俯视分解图如图3 (a)和(b)所示,1-模拟眼前部件保护罩、2-模拟眼前部件主体、3-固定螺丝孔、4-用于检测视场角参数的阶梯状同心圆环、5-模拟眼后部件主体、6-弯月透镜和弯月透镜镜架、7-双凸透镜和双凸透镜镜架、8-密封圈、9-注水孔、10-用于置放三维分辨率板的凹槽、11-用于放置平行玻璃片的空室。其中,光学玻璃与镜架均胶接密封;弯月透镜镜架与模拟眼前部件边缘处紧贴、胶接密封;双凸透镜镜架与模拟眼前部件采用螺纹匹配安装,方便不同屈光度模拟眼晶状体的更换;模拟眼后部件与模拟眼前部件由螺丝固定、胶圈密封。为了保证房水充满组织液,需贯通房水和玻璃体腔,双凸透镜镜架中心圆放置晶状体,边缘四个圆为贯通的通孔,方便组织液流通,如图3 (b)分解部件7所示。

图 3 所设计眼模型的(a)机械结构剖视图、(b)实物俯视分解图和(c)装配图
Figure 3. Designed eye model: (a) Sectional view of mechanical structure, (b) top view of real device and (c) assembling drawing
模拟眼后部件应包含分辨率、视场角、深度测量准确性和图像匹配度参数的检测方法。镜筒后部件曲面加工多个阶梯状同心圆环,视场标尺起始值60°、格值10°、最大视场角测试范围110°,可满足市面上绝大多数眼科OCT的视场角检测;相比ISO 16971中提出的单根细丝测试图像匹配度,该眼模型采用十字交叉的两根光纤来测试眼科OCT设备X和Y方向的图像匹配程度,将带圆形金属边框的十字叉丝组件卡在最靠近眼底的台阶内;深度测量准确性参数和分辨率参数检测无法集成于一个眼模型内,需根据测试需求将三维分辨率板或平行玻璃板组件安装到眼底凹槽中,分别实现OCT设备分辨率和深度测量准确性参数的测试。镜筒后部件的注水孔可将水或其他折射率液体注入密封的模拟眼,用于模拟前房和玻璃体组织液。
模拟眼镜筒后部件加工标准M4和M6螺纹孔,可与通用的光学组件配合,实现模拟眼的固定。除此之外,还针对眼科光学设备的颚托设计了专用可调机械底座,不仅能够将模拟眼与颚托固定,可实现模型眼高度、入射角度的调节,确保模拟眼视轴与眼科OCT设备光轴共轴,整套装置效果图如图3 (c)所示。
-
Renishaw共焦拉曼显微镜(型号:Invia)可对微小样品微区结构、成分、面貌进行分析鉴定,横纵向分辨力分别为0.5 μm和1.5 μm;配备高精度三维微位移台(三个方向行程均为0~100 μm、定位精度0.5 μm),经过校准溯源,确定该平台三个方向的位移误差不超过±0.1 μm;可对3D打印分辨率板的线宽及高度进行溯源。对用于计量横向分辨率参数的1~6号测试靶标中三对横向与纵向排列的线宽及线对间距进行溯源,为保证测试准确性,每个线对宽度及线对间隔进行三次测量并取总体平均值,溯源结果如图4 (a)所示;对用于计量轴向分辨率参数的1~5号测试靶标线对高度进行溯源,为保证测试准确性,每个线对高度进行三次测量并取平均值,溯源结果如图4 (b)所示。由图4 (a)可见,横向线宽尺寸均低于设计值,这是由于光敏树脂材料在3D打印过程中固化收缩,导致横向尺寸减小。由图4 (b)可见轴向尺寸也存在相同情况,导致溯源结果略小于设计尺寸。但由于光敏树脂固化收缩率趋于稳定,可用溯源结果作为分辨率参数的判断值进行评价,并不影响模拟眼的计量性能。
-
Nikon投影仪,X轴方向行程150 mm、Y轴方向行程100 mm、步进精度1.5 µm,可对阶梯状同心圆环的横向尺寸进行溯源,再结合测得的模拟眼后半球直径,即可计算出各个同心圆环所对应的视场角。需要说明的是,文中计算的视场角与ISO 16971中定义的FOV略有不同,为了与大多数眼科OCT设备厂商标称的设备视场角相对应,使用模拟眼球心位置作为参考点,与阶梯状圆环连线的张角即定义为其对应的视场角。同心圆环由内至外编号ID为1~6,通过三次测试取平均值作为测试结果,如表2所示,结合模拟眼后半球直径溯源结果24 mm,即可计算得出模拟眼1~6号圆环所对应的视场角。
表 2 模型眼视场角参数溯源
Table 2. Tracing results of FOV of model eye
Concentric rings ID Nominal diameter/
mmTest results/
mmNominal FOV/
(°)Test results/
(°)1 12 12.255 60 61.41 2 13.77 13.834 70 70.40 3 15.43 15.499 80 80.45 4 16.97 17.035 90 90.44 5 18.39 18.468 100 100.62 6 19.66 19.543 110 109.03 -
使用视微影像(河南)科技有限公司的VG100D眼科光学相干断层成像设备作为测试设备,设备标称值:横向分辨率小于20 μm,轴向分辨率小于6.3 μm,最大视场角77°,最大成像深度2.7 mm。
将模拟眼置于眼科OCT设备物方处,调整模拟眼的姿态与眼科OCT设备的相对位置,使得模型眼的光轴与眼科OCT设备的光轴重合并清晰成像。使用眼科OCT设备对镜筒后部件十字叉丝观测,测试图像匹配度;对阶梯状同心圆环观测,记录视场边缘对应的圆环ID,测试视场角范围;读取能清晰分辨的横向分辨率线对数作为横向分辨率指标的检测结果;读取能清晰分辨高低起伏的轴向分辨率线对数作为轴向分辨率指标的检测结果;测试玻璃片前后表面距离,计算玻璃片实测厚度,评估设备深度测量准确性。
-
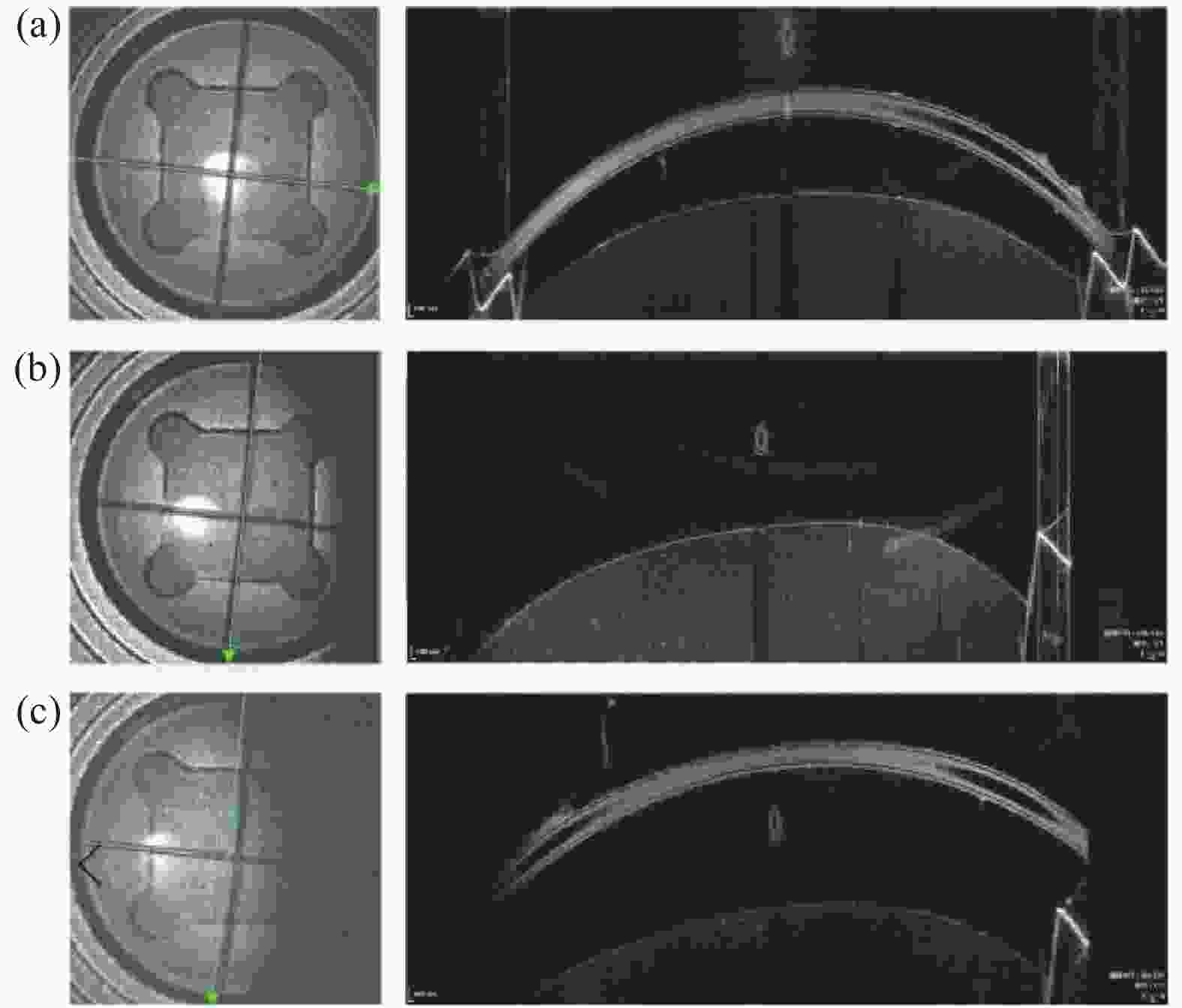
为了验证两根垂直交叉的光纤测试图像匹配度方法更全面,在实验中调整样机Y方向图像匹配偏移量200 μm后开始测试。如图5 (a)所示,扫描线对准X方向光纤,可清晰呈现光纤完整的剖面结构,图像匹配;如图5 (b)所示,扫描线对准Y方向光纤,不能呈现细丝剖面结构,图像不匹配;如图5 (c)所示,当尝试扫描线偏移Y方向细丝一定距离,才可清晰呈现光纤完整的剖面结构,由此可以判定,设备在X方向图像匹配,Y方向图像不匹配,所以仅用一根细丝评价图像匹配程度并不全面。实验用光纤的溯源结果为125 μm,将扫描线对准光纤中部进行测试,则图像匹配度测试的误差最小可以达到62.5 μm。
-
选取多线扫描模式,选择扫描线对准横向分辨率线对,由于每组测标由三对横向与纵向垂直排列的长条图案组成,1~6号中水平排布的线对可一次测得,测试结果及扫描位置示意图如图6 (a)所示,自右向左红框中标记的为第1~6号线对,同时显示B-scan扫描方向在三维分辨率板的对应扫描位置。可清晰观测到第1~4号线对图呈亮暗分布,不可清晰观测到第5~6号线对呈亮暗分布,可初步判断设备的分辨率介于4号线对和5号线对之间。对纵向分布的4~5号线对进行单独扫描,如图6 (b)、6 (c)所示,再对线对的中心位置进行灰度值扫描,其结果如图6 (d)、 (e)所示。以两条明条纹的半高全宽位置不重合为设备是否能分辨两条明条纹的判断依据,故设备可分辨的横向分辨率线对为4号,不可分辨的横向分辨率线对为5号,其横向分辨率介于12.2~17.5 μm之间,则设备标称横向分辨率小于20 μm合格。

图 6 横向分辨率测试结果及其扫描位置示意图:(a)横向1~6号线对;(b)纵向4号线对;(c)纵向5号线对;(d)纵向4号线对灰度图;(e)纵向5号线对灰度图
Figure 6. Test results for lateral resolution and its scanning location diagram: (a) Horizontal No. 1-6 line pairs; (b) Vertical No. 4 line pair; (c) Vertical No. 5 line pair; (d) Grey-scale map of vertical No. 4 line pair; (e) Grey-scale map of vertical No. 5 line pair
将扫描线对准轴向分辨率台阶,测试结果如图7 (a)所示,自左向右红框中标记的为第1~5号台阶,同时显示B-scan扫描方向在三维分辨率板的扫描位置。进一步对分辨率台阶1~5进行了二值化取值并拟合如图7 (b)所示,可以更加直观地观测到各个台阶凸起的程度。以最高点与最低点的中心位置像素距离为设备是否能分辨分辨率台阶的判断依据,设置三个像素为判定标准。如图7 (c)所示,5号台阶与基底的像素距离为5.4,则说明设备的轴向分辨率可以分辨5号台阶,则设备标称的轴向分辨率小于6.3 μm合格。若要测试横向或轴向分辨率更准确的范围,可以方便地使用3D打印技术,根据需要制作多种尺寸的分辨率板,覆盖更多尺寸,缩小相邻线对尺寸的差距。
-
将扫描线通过模拟眼中心,扫描同心圆环测试结果如图8 (b)所示。将其对应于模型眼剖面,如图8 (a)所示,可观测到第二个圆环,不可观测到第三个圆环,得到设备的视场角介于70.40°~80.45°之间,则设备标称的最大视场77°合格。
-
深度测量准确性是通过测试玻璃片前后表面距离,与玻璃片实际厚度进行比较,计算其误差是否满足国际标准ISO 16971中规定的深度测量允差在±3%之内。实验用平行玻璃片中心厚度区域(5 mm×5 mm)溯源值为1.000 mm,测量不确定度小于5 μm。深度测试结果如图9 (a)所示,因设备内部预设折射率与玻璃片实际折射率不一致,但其总光程是一样的,故通过公式(4)换算出设备对平行玻璃片的实际测试结果:

图 9 深度测试结果:(a) OCT设备扫描图像和(b)数据处理后的图像
Figure 9. Results for depth measurement: (a) Scanning image of OCT equipment and (b) image after data processing
$$ {n_{dev}} \cdot {l_{dist}} = {n_{mir}} \cdot {l_{mir}} $$ (4) 式中:ndev=1.33为VG100D眼科OCT设备预设人眼分辨率群折射率;ldist为OCT设备程序处理得到的上下表面距离,如图9 (b)所示;nmir=1.525[18](波长830 nm)为H-K9 L材料折射率;lmir为换算后的OCT设备玻璃实测厚度。
对平行玻璃片中心进行多次测量取平均ldist=1.174 mm,通过公式(4)计算得出lmir=1.024 mm。使用同样的方法重复测量五次,最终测试平均值满足深度测量允差±3%,故设备深度测量准确性符合要求。
综上所述,文中设计的模型眼可以对眼科OCT设备的横向分辨率、轴向分辨率、视场角、图像匹配度、深度测量准确性参数进行评估和测试,且操作简单、集成度高、适用范围广、稳定性强,可广泛用于眼科OCT设备的计量校准。
-
文中以国际标准ISO 16971提出的测量方案为基础,同时参考Gullstrand I号模型眼,结合微纳3D打印技术,设计并研制了一种模拟真实人眼结构的计量校准用眼模型。该模拟眼与测试OCT设备相关的设计参数均可溯源,适用于评估眼科OCT设备的横向分辨率、轴向分辨率、视场角、图像匹配度、深度测量准确性等多个关键参数,能确保眼科OCT设备输出量值的准确性和有效性。使用已标定的模拟眼对商用眼科OCT设备进行了测试,相比ISO 16971国际标准推荐的测试装置有以下几个方面的提升:(1) 图像匹配度参数测试采用十字叉丝代替推荐的一根细丝,可实现X、Y方向图像匹配度同时测试,测试结果更加准确可靠;(2) 横向分辨率的测试采用了3D打印具有一定高度的分辨率线对代替推荐的在一块玻璃平板上表面加工1951 USAF分辨率线对,能通过一张B-scan图进行横向分辨率的测试,而不需要启用3D扫描模式去沿轴向寻找平面分辨率板对应的C-scan图像,且该图像会发生弯曲,影响分辨率测试准确性;(3) 纵向分辨率的测试采用3D打印高度不同的台阶代替通过测试玻璃反射信号的半高宽来测试,能直观地通过B-scan图像获得设备的实际成像分辨率水平,相比通过测试玻璃反射信号更加准确且不需要进入设备开发者模式读取原始信号数据;(4) 视场角参数通过测量阶梯状分布的同心圆环代替测量沿X、Y方向标定尺寸的平面玻璃实现,通过一张B-scan图即可实现设备视场角的评价,且避免了平面图像的弯曲变形,影响测试的准确性。
将微纳3D打印技术应用于计量校准装置中能实现普通机械加工工艺难以完成的复杂计量模型制造,尤其是复杂微结构的加工制作。随着3D打印技术的不断发展,在打印分辨率、精度和重复性等方面将进一步提升,其在计量校准装置的加工方面具有巨大的潜力。
Development of metrology and calibration devices for ophthalmic OCT equipment based on 3D printing technology
-
摘要: 为了评估眼科光学相干断层成像(OCT)设备的分辨率、视场角、图像匹配度、深度测量准确性等多个关键参数,确保设备输出量值的准确性与有效性,设计并研制了一种模拟真实人眼结构且参数可溯源的模拟眼,包含角膜和晶状体等人眼主要屈光结构。设计并依托3D打印技术加工了用于横向与轴向分辨率检测的三维分辨率板;设计加工了用于视场角检测的阶梯状同心圆环结构;同时设计加工了用于图像匹配度检测的交叉光纤组件和用于深度测量准确性参数检测的平行玻璃板组件,可适配于模拟眼眼底凹槽内。使用共焦拉曼显微镜对三维分辨率板尺寸溯源,横向和轴向最小可检测分辨率分别为9.7 μm和5.7 μm;使用尼康投影仪对同心圆环尺寸及光纤直径溯源,最大可检测视场角109.03°以及最小62.5 μm的图像匹配度检测;使用尼康高度计对平行玻璃板中心厚度溯源,其测量不确定度小于5 μm。经过对商用眼科OCT设备测试表明,结合微纳3D打印技术的计量校准用模拟眼具有精度高、集成度高、适用范围广、稳定性强等优点,适用于眼科OCT设备的计量校准。Abstract: To evaluate the resolution, angular field of view (FOV), coalignment of fundus images and OCT scans, depth scaling and other key parameters of optical coherence tomography (OCT) equipment and ensure the accuracy and validity of the equipment output values. In this paper, a model eye simulating real human eye structure was designed and developed, including the main refractive structures, such as cornea and lens, and its parameters are traceable. A 3D resolution board for lateral and axial resolution detection was designed and fabricated based on 3D printing technology. A stepped concentric ring structure was designed and machined for FOV detection. At the same time, the cross fiber module for image matching detection and the parallel glass module for depth scaling detection were designed and manufactured, which can be adapted to the fundus groove of the model eye. Confocal Raman microscopy was used to trace the size of the 3D resolution board, and the minimum detectable values for lateral and axial resolutions were 9.7 μm and 5.7 μm, respectively. The sizes of the concentric rings and fiber diameter can be traced by a Nikon projector. The maximum detectable FOV is 109.03°, and the image matching minimum accuracy is 62.5 μm. The center thickness of the parallel glass plate was traced by a Nikon digital height gauge, and the measurement uncertainty was less than 5 μm. The test of commercial ophthalmic OCT equipment showed that the model eye metrology and calibration device based on 3D printing technology has the advantages of high accuracy, high integration, wide application range and strong stability, so it is suitable for metrology and calibration of ophthalmic OCT equipment.
-
Key words:
- ophthalmic OCT /
- model eye /
- metrology and calibration /
- 3D printing technology
-
图 6 横向分辨率测试结果及其扫描位置示意图:(a)横向1~6号线对;(b)纵向4号线对;(c)纵向5号线对;(d)纵向4号线对灰度图;(e)纵向5号线对灰度图
Figure 6. Test results for lateral resolution and its scanning location diagram: (a) Horizontal No. 1-6 line pairs; (b) Vertical No. 4 line pair; (c) Vertical No. 5 line pair; (d) Grey-scale map of vertical No. 4 line pair; (e) Grey-scale map of vertical No. 5 line pair
表 1 所设计的眼模型主要参数
Table 1. Main parameters of designed eye model
Eyeball tissue Parameters Radius of curvature Thickness Refractive index Anterior surface of cornea 7.60 0.50 1.526 Posterior surface of cornea 4.90 Anterior chamber - 2.41 1.333 Anterior surface of lens 10.46 4.50 1.526 Posterior surface of lens −12.73 Vitreous - 17.63 1.333 Retina −12.50 - - 表 2 模型眼视场角参数溯源
Table 2. Tracing results of FOV of model eye
Concentric rings ID Nominal diameter/
mmTest results/
mmNominal FOV/
(°)Test results/
(°)1 12 12.255 60 61.41 2 13.77 13.834 70 70.40 3 15.43 15.499 80 80.45 4 16.97 17.035 90 90.44 5 18.39 18.468 100 100.62 6 19.66 19.543 110 109.03 -
[1] Huang D, Swanson E A, Lin C P, et al. Optical coherence tomography [J]. Science, 1991, 254(5035): 1178-1181. doi: 10.1126/science.1957169 [2] Minakaran N, de Carvalho E R, Petzold A, et al. Optical coherence tomography (OCT) in neuro-ophthalmology [J]. Eye, 2021, 35(1): 17-32. doi: 10.1038/s41433-020-01288-x [3] Liu Z, Saeedi O, Zhang F, et al. Quantification of retinal ganglion cell morphology in human glaucomatous eyes [J]. Investigative Ophthalmology & Visual Science, 2021, 62(3): 34. [4] Everett M, Magazzeni S, Schmoll T, et al. Optical coherence tomography: From technology to applications in ophthalmology [J]. Translational Biophotonics, 2021, 3(1): e202000012. [5] Hammer D, Villanueva R, Agrawal A, et al. Distribution of inner limiting membrane microglia in glaucoma measured with adaptive optics-optical coherence tomography [J]. Investigative Ophthalmology & Visual Science, 2020, 61(7): 3498. [6] Tomlins P H, Ferguson R A, Hart C, et al. Point-spread function phantoms for optical coherence tomography[R]. Middlesex: National Physical Laboratory, 2009. [7] Agrawal A, Pfefer T J, Gilani N, et al. Three-dimensional characterization of optical coherence tomography point spread functions with a nanoparticle-embedded phantom [J]. Optics Letters, 2010, 35(13): 2269-2271. doi: 10.1364/OL.35.002269 [8] Pfefer J, Fouad A, Chen C W, et al. Multi-system comparison of optical coherence tomography performance with point spread function phantoms [C]//Design and Quality for Biomedical Technologies VI. International Society for Optics and Photonics, 2013, 8573: 85730 C. [9] Hu Zhixiong, Liu Wenli, Hong Baoyu, et al. A physical model eye with 3D resolution test targets for optical coherence tomography [J]. Opto-Electronic Engineering, 2014, 41(12): 28-32, 38. (in Chinese) [10] Cao Z, Ding Z, Hu Z, et al. Model eyes with curved multilayer structure for the axial resolution evaluation of an ophthalmic optical coherence tomography device [J]. Journal of Innovative Optical Health Sciences, 2018, 11(3): 1850013. doi: 10.1142/S179354581850013X [11] Hu Zhixiong, Hao Bingtao, Liu Wenli, et al. Research on point spread function phantom fabrication and application for evaluating resolution performance of OCT systems [J]. Acta Optica Sinica, 2015, 35(4): 0417001. (in Chinese) [12] Wang H, Liu W, Hu Z, et al. Model eye tool for retinal optical coherence tomography instrument calibration [J]. Journal of Innovative Optical Health Sciences, 2021, 14(3): 2150010. doi: 10.1142/S1793545821500103 [13] International Organization for Standardization. ISO 16971: 2005 Ophthalmic instruments-Optical coherence tomograph for the posterior segment of the human eye [S]. 2015. [14] Kedia N, Liu Z, Sochol R D, et al. 3-D printed photoreceptor phantoms for evaluating lateral resolution of adaptive optics imaging systems [J]. Optics Letters, 2019, 44(7): 1825-1828. doi: 10.1364/OL.44.001825 [15] Lamont A C, Restaino M A, Alsharhan A T, et al. Direct laser writing of a titanium dioxide-laden retinal cone phantom for adaptive optics-optical coherence tomography [J]. Optical Materials Express, 2020, 10(11): 2757-2767. doi: 10.1364/OME.400450 [16] Horng H, O ’Brien K, Lamont A, et al. 3D printed vascular phantoms for high-resolution biophotonic image quality assessment via direct laser writing [J]. Optics Letters, 2021, 46(8): 1987-1990. doi: 10.1364/OL.412849 [17] Aumann S, Donner S, Fischer J, et al. Optical Coherence Tomography (OCT): Principle and Technical Realization[M]//Bille J. High Resolution Imaging in Microscopy and Ophthalmology. Cham: Springer, 2019: 59-85. [18] Refractive Index. INFO [EB/OL]. [2021-12-20]. https://refractiveindex.info/?shelf=glass&book=CDGM-K&page=K4A. -





 下载:
下载: